近些年,随着血管内支架置入术在下肢动脉硬化闭塞等疾病中的应用日益广泛[1],支架内再狭窄(ISR)作为一个新的且难以处理的问题而出现[2]。尽管近年来随着腔内减容理念的不断推广,以及药物涂层球囊(drug-coated balloon,DCB)的应用也在一定程度上降低了支架的置入率,但ISR的治疗仍然是一个棘手的问题[3]。
虽然腔内的各种技术如球囊扩张和支架置入已经在ISR的治疗中得到应用[4],但实际的随访效果欠佳[5]。腔内减容和DCB在处理复杂的ISR病变中有着各自的局限性,将两种技术结合起来,理论上会取得满意的结果。本中心自2017年5月—2018年5月采用腔内减容联合DCB的联合技术治疗复杂性股腘动脉支架内再狭窄患者21例,近期的随访效果满意,现报告如下。
1 资料与方法
1.1 一般资料
对我院2017年5月—2018年5月采用联合技术治疗的ISR患者的临床资料进行统计分析,共纳入21例患者,其中男13例(61.9%),女8例(38.1%);年龄52~86岁,平均(69.8±11.0)岁。术前踝肱指数(ankle brachial index,ABI)为0.45±0.14、下肢CT血管成像(CTA)判定支架再狭窄的部位,并分析斑块是否稳定。其中间歇性跛行11例,静息痛5例,足部溃疡或坏疽2例,距上次支架置入时间为2~26个月,平均为(7.9±2.5)个月。21例患者其他临床病理因素见表1。
表1 患者的一般资料
Table 1 The general data of the patients
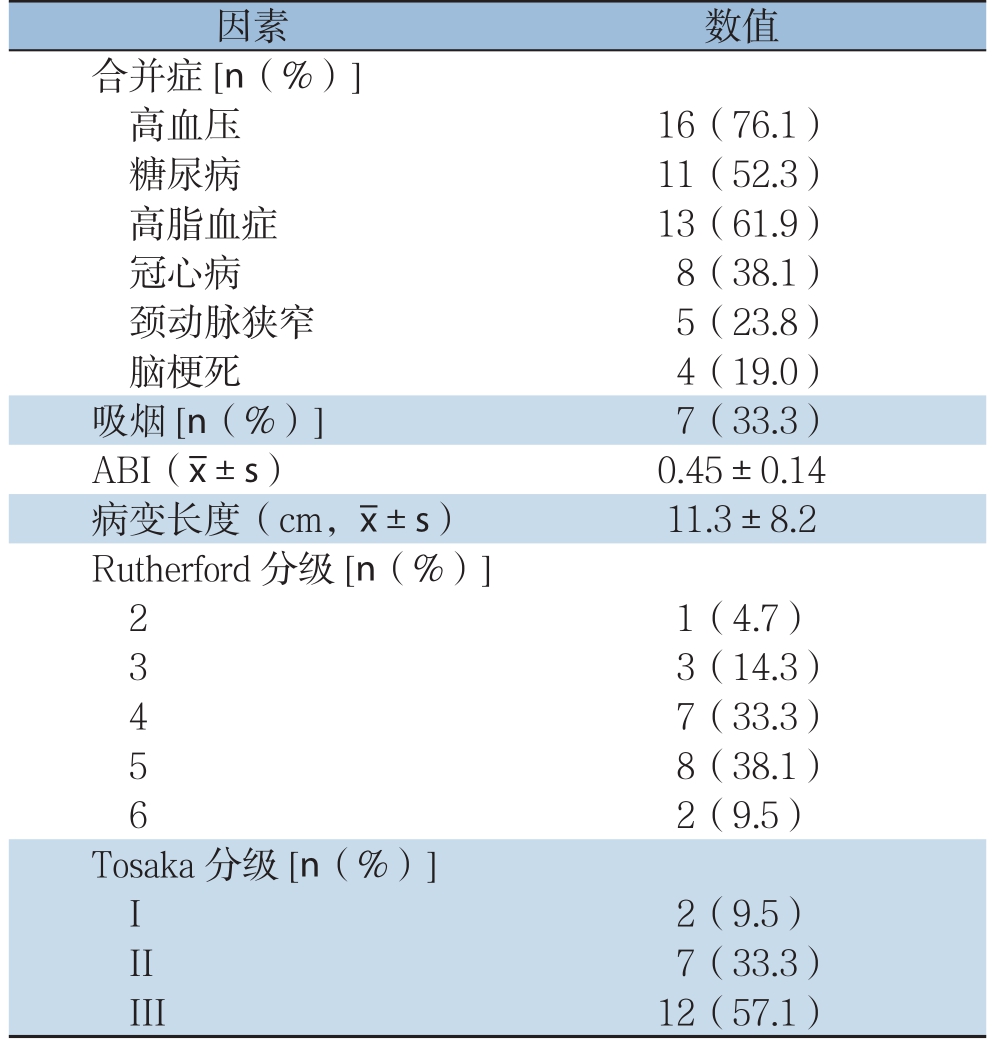
因素 数值合并症[n(%)]高血压 16(76.1)糖尿病 11(52.3)高脂血症 13(61.9)冠心病 8(38.1)颈动脉狭窄 5(23.8)脑梗死 4(19.0)吸烟[n(%)] 7(33.3)ABI(x±s) 0.45±0.14病变长度(cm,x±s) 11.3±8.2 Rutherford分级[n(%)]2 1(4.7)3 3(14.3)4 7(33.3)5 8(38.1)6 2(9.5)Tosaka分级[n(%)]I 2(9.5)II 7(33.3)III 12(57.1)
病例纳入标准:⑴年龄为18~85岁既往接受过股腘动脉支架置入的患者;⑵Rutherford分级2~6级;⑶靶血管直径为4~8 mm,靶病变血管长度必须>1 cm且<25 cm;⑷患肢的ABI<0.8;⑸影像学检查:至少有1项影像学显示股腘动脉ISR,并且数字减影血管造影(DSA)检查证实支架内狭窄程度≥50%[6];⑹膝下至少有1支非闭塞血管开放至足部。排除标准:⑴肝、肾、心、脑等基本器官严重功能障碍的患者;⑵腔内治疗禁忌证,如凝血功能障碍的患者;⑶对造影剂、紫杉醇过敏或抗凝、抗血小板治疗有禁忌证;⑷在治疗髂动脉或股总动脉的流入病变后,仍有直径> 50%的狭窄;⑸支架断裂[7];⑹病变肢体计划截肢和预期寿命<1年。
1.2 TurboHawk腔内减容联合DCB的治疗ISR方法
取腹股沟区浸润麻醉,根据术前影像学检查选择合适的穿刺途径。植入5~7 F血管鞘后,经翻山鞘造影确认ISR病变的部位及程度(图1A)以及膝下动脉血管造影情况(图1B),并选择合适型号的TurboHawk斑块切除导管。在全身肝素化后,软导丝配合单弯导管通过病变段,对于严重狭窄或闭塞的病变,则使用0.014 in微导丝配合微导管或直接使用V-18导丝通过病变段,接着再次造影观察是否在真腔内操作,引入ev3 SpiderFX保护伞,根据路图,TurboHawk斑块切除系统通过保护伞导丝被缓慢推入并切割病变段血管,如病变狭窄较重且旋切导管难以通过时,则可以用适当型号的小球囊进行预扩张,然后再由近端向远端缓慢切割,最后返回到病变的近端(图1C),多角度操作3~5次后及时清除旋切装置收集槽内的小斑块,重复相关操作直至复查造影显示管腔好转,局部无夹层形成但存在散在中度狭窄。DCB扩张前先选择普通球囊递增扩张,然后选择合适型号(球囊长度一般覆盖支架全程,并超过支架近远端1 cm)的紫杉醇DCB行支架内扩张,维持扩张时间为3 min(图1D),待造影显示残余狭窄≤30%时(图1E)撤出保护伞(图1F),若造影显示残留狭窄或限流性夹层,且在二次球囊扩张后仍未取得较好的管腔通畅性,可考虑行支架置入术。术后给予低分子肝素4 000 U皮下注射(2次/d,共3 d),并口服(阿司匹林100 mg/d、氯吡格雷75 mg/d)3个月,3个月后若无禁忌证可终生单药维持治疗。
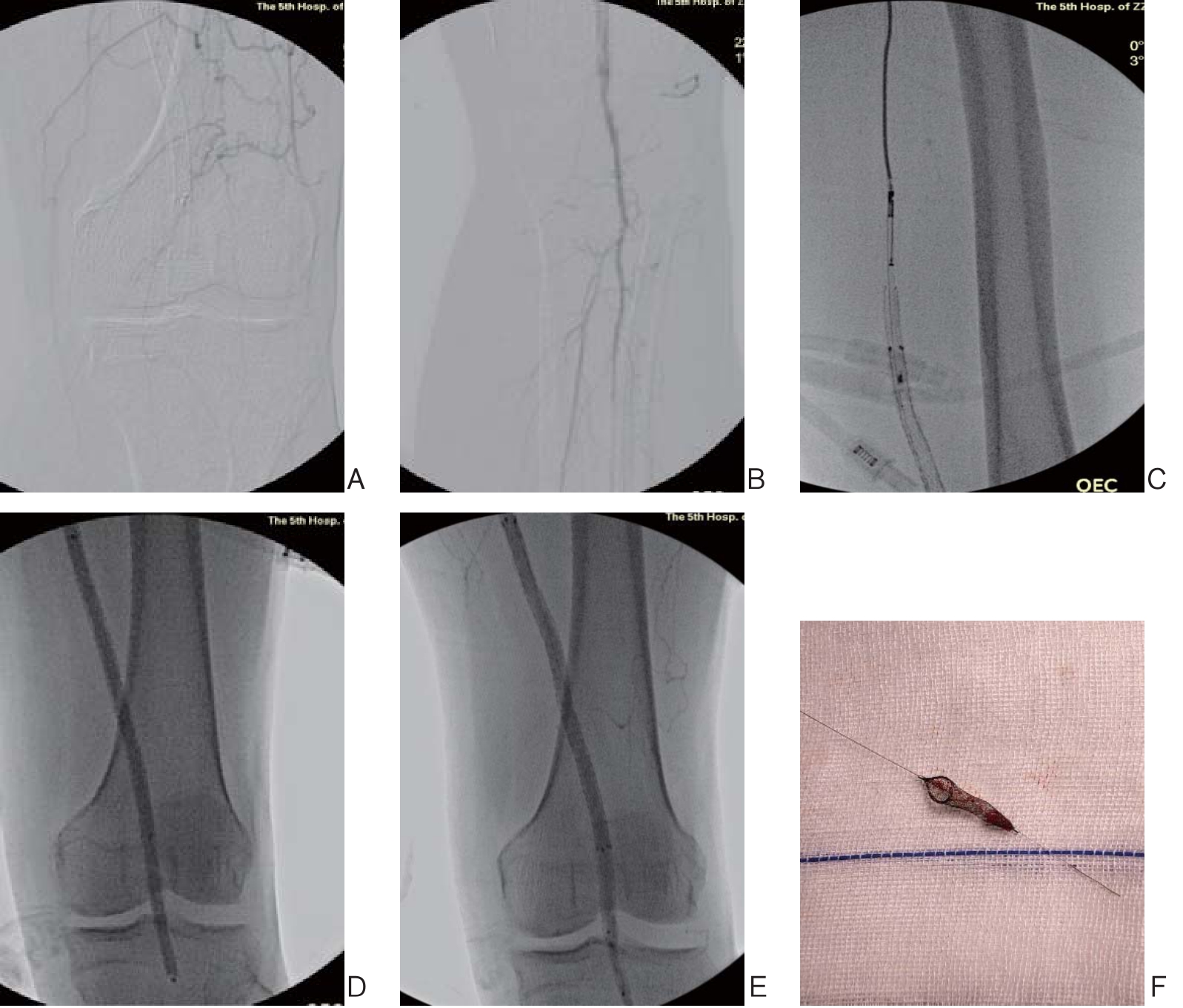
图1 术中相关照片 A:支架闭塞情况;B:膝下动脉造影显示;C:TurboHawk斑块旋切系统退回至病变近心端;D:DCB扩张支架内病变;E:术后造影显示残余狭窄<30%;F:术后可见保护伞内脱落的斑块碎屑
Figure 1 Intraoperative images A:View of the stent occlusion B:View of the infrapopliteal artery;C:TurboHawk system returned to the proximal end of the lesion;D:The DCB expanding in-stent lesions;E:Postoperative angiography showing the restoration of normal blood fl ow and the residual stenosis less than 30%;F:Plaque debris present in the embolic protection device after its withdrawal
1.3 随访
对21例采用联合技术治疗的患者进行随访。术后6个月和12个月复查多普勒超声和ABI。当间歇性跛行等症状再次出现或超声多普勒检查怀疑再狭窄时,进行CTA或磁共振血管成像,必要时进行血管造影重新评估。本技术成功的定义为经联合技术治疗后的管腔残余狭窄<30%,且病变部位无血管穿孔或远端栓塞;一期通畅率一般定义为在随访期间,治疗段的血管没有闭塞或明显的再狭窄,且无需再次干预;免于临床驱动的 靶病变血运重建率(freedom from CD-TLR),其中临床驱动的靶病变血运重建率CD-TLR指的是由症状、ABI下降≥20%或与基线相比>0.15引起的再次干预)[8]。
1.4 统计学处理
采用SPSS 23.0软件对数据进行分析和处理。计量资料用均数±标准差( ±s)表示。采用配对t检验分析手术前后ABI的变化,P<0.05为差异有统计学意义。Kaplan-Meier生存分析用于表示随访12个月时的一期通畅率和免于靶病变血运重建率。
±s)表示。采用配对t检验分析手术前后ABI的变化,P<0.05为差异有统计学意义。Kaplan-Meier生存分析用于表示随访12个月时的一期通畅率和免于靶病变血运重建率。
2 结果
2.1 早期结果
所有21例患者均取得了技术和程序上的成功。未发生与手术相关的不良事件(无穿孔、动静脉瘘和假性动脉瘤),住院期间未发生重大心、脑血管事件。21例患者术后的Rutherford分级:0级2例(9.5%),1级9例(42.8%),2级3例(14.2%),3级1例(4.7%),4级3例(14.2%),5级3例(14.2%)。ev3-SpiderFX保护伞用于膝下只有单支血管通畅的患者,其中4例拦截了少量脱落碎片。2例(9.5%)患者经历远端栓塞,其通过额外的球囊扩张和/或血栓溶解解决,有1例(4.7%)患者由于严重的限流夹层(≥D级),需要补救支架置入术。
2.2 随访结果
在12个月的随访期间,1例(4.7%)随访至7个月时因心力衰竭而死亡,1例(4.7%)在随访至9个月时因冠心病而死亡,1年内全因和心血管病死率为9.4%;1例失访,18例(85.7%)完成了12个月的随访。18例患者在12个月时为0.69~1.45,平均0.84±0.12,与术前比较差异有统计学意义(P<0.05),表明血流动力学的成功,且随访期间未出现截肢及与手术相关的死亡病例。Kaplan-Meier生存分析表明12个月的一期通畅率为83.3%(15/18),12个月时免于临床驱动的靶病变血运重建率为88.9%(16/18)(图2)。在Tosaka I级和II级共有8例患者完成了12个月的随访,并且10例在Tosaka III级完成了12个月的随访。Tosaka I级和II级12个月的一期通畅率为87.5%(6/8),Tosaka III级为90.0%(9/10),差异无统计学意义(P>0.05)。在随访至12个月时,Tosaka I级和II级免于临床驱动的靶病变血运重建率87.5%(7/8),Tosaka III级为90.0%(9/10),差异无统计学意义(P>0.05)。在随访期间,对于再次出现管腔狭窄的患者,其中1例再次给予DCB扩张,另1例行裸支架置入。
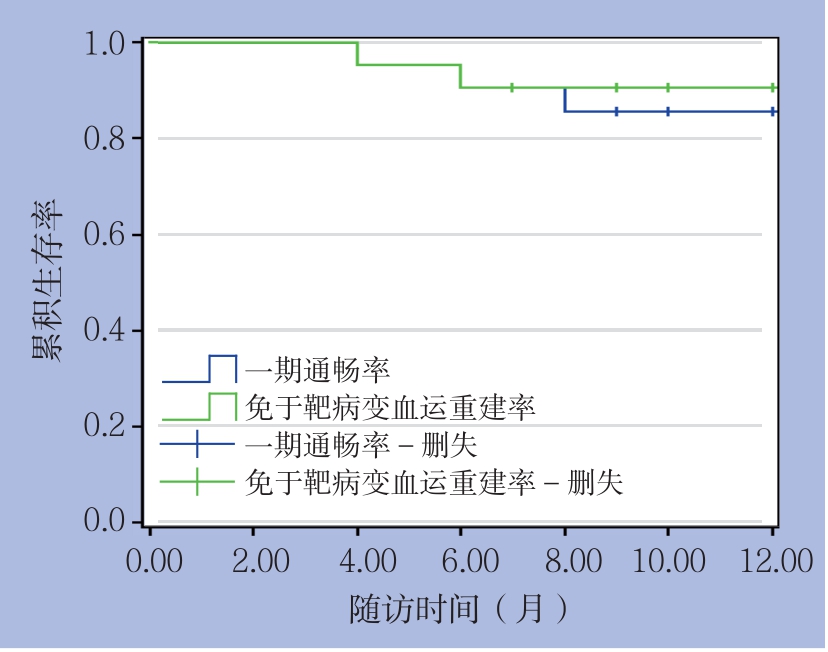
图2 18例患者术后一期通畅率及免于靶病变血运重建率
Figure 2 Primary patency rate and freedom from CD-TLR in the 18 patients after operation
3 讨论
目前支架置入已经普遍应用于股腘动脉狭窄或闭塞病变,支架置入后存在弹性回缩、残余狭窄以及限流性夹层的问题,同时支架内再狭窄的发生率也在逐年上升,1年内高达15%~32%[3]。近年来,有许多腔内的治疗方法可用于治疗股腘动脉ISR,例如球囊扩张,再次支架置入,或各种腔内减容技 术[9]。总的来说,当下没有针对股腘动脉ISR的最佳治疗方法[10]。
用普通球囊重复扩张来治疗ISR曾经是治疗股腘动脉ISR最主要的方法,术后即刻通畅率较高,但不幸的是,中期和长期随访结果结果令人失望[11]。在处理原发下肢动脉硬化病变时,切割球囊有一定理论上的优势,球囊上的小刀片随着球囊的扩张来切割增生的斑块,从而减少球囊扩张时内膜成分的滑脱及新生内膜的形成,然而,其对股腘动脉ISR治疗的效果不令人满意。Dick等[12]报告39例经切割球囊与经普通球囊治疗股腘动脉ISR的随访效果,切割球囊血管成形术组在6个月时的再狭窄率为65%,而普通球囊血管成形术组为73%(P=0.73),说明切割球囊对于ISR的治疗与普通球囊相比,其实际的临床优势不太显著。目前市面上有3种类型的支架可用于处理股腘动脉ISR病变,分别是金属裸支架,覆膜支架和药物洗脱支架[13],但支架再次置入在股腘动脉ISR治疗中的中远期疗效尚未得到充分证实,同时支架的再次置入会缩小管腔的直径,为以后的二次干预增加了难度。许多专家建议在股腘动脉ISR患者的治疗过程中尽量避免重复的支架置入。
从理论上讲,减容技术可以去除腔内增生的内膜和细胞外基质,从而扩大管腔的内径[14]。目前常用的腔内减容技术有很多,但不管哪种技术,在减容的同时,都会对内膜造成不同程度的刺激,而产生一定的增生[15]。定向腔内斑块切除术通过旋转的刀片去除斑块,并且移除的斑块没有被抽吸,而是收集在锥形管中。DEFINITIVE LE研究[16]是一项关于定向腔内斑块切除术的研究,纳入了800例患者,共1 022处病变,其中743处有跛行,279处为严重下肢缺血;跛行组中,72.1%的患者是SFA段病变,15.3%是腘动脉病变,12.5%为膝下动脉病变,平均病变长度为(7.4±5.3)cm。主要终点是12个月时的一期通畅率(跛行患者为78%,严重肢体缺血患者为71%),无意外大截肢(95%),补救支架置入率为3.2%。对糖尿病患者亚组的分析显示,糖尿病亚组与非糖尿病亚组两组之间免于TLR率(分别为77%、78%)。由此表明减容技术治疗下肢动脉硬化闭塞症安全有效,且糖尿病与非糖尿病均可得到良好的疗效。
支架内再狭窄主要的生理机制是平滑肌细胞增殖而引起的内膜增生,为了减少新生内膜的形成,关键是要抑制平滑肌细胞的增殖[17]。紫杉醇已被证明可抑制新生内膜的生长,从而减少再狭窄,因此人们对DCB作为解决股腘动脉ISR寄予了很大的期待[18]。在DEBATE-ISR研究[19]中,将44例使用DCB与44例普通球囊治疗股腘动脉ISR的患者进行比较,随访12个月后DCB组有19.5%(8/41)的患者再次出现再狭窄,而普通球囊组复发再狭窄为71.8%(28/39)(P<0.001),1年的TLR分别为13.6%和31.0%(P<0.001)。然而,在3年的随访中,DCB组的TLR率为40%,而常规PTA组为43%(P=0.8);Kaplan-Meier分析显示两组间免于TLR率无显着差异。因此,在股腘动脉ISR中使用DCB后长期的反复发生再狭窄仍是一个需要考虑的问题。
基于以上研究结果,尽管已提出各种治疗策略作为股腘动脉ISR的治疗方法,但中长期随访的的复发狭窄率仍是居高不下。本中心采用腔内减容联合DCB的联合技术治疗股腘动脉ISR 21例,尝试通过TurboHawk旋切导管尽可能多地去除斑块,并且使用普通球囊预扩张来辅助DCB的扩张,并获得了令人满意的初步结果。随访至12个月时ABI为0.69~1.45,平均0.84±0.12(P<0.05)。术后12个月时一期通畅率为83.3%(15/18),12个月时免于临床驱动的靶病变血运重建率为88.9%(16/18)。临床症状均得到改善,未发生与手术相关的不良事件,近期效果让人满意。van den Berg等[20]回顾性分析了14例ISR患者(78.6%为Tosaka III型病变),均行激光减容联合DCB的联合技术,随访19个月,仅有1例再次出现ISR,一期通畅率为91.7%,效果满意。Gandini等[6]也进行了相似的试验,纳入了48例患者(均为Tosaka III型病变),在激光消融联合DCB组中,6个月和12个月的通畅率(分别为91.7%和66.7%)显着高于仅DCB组(P=0.01)(分别为58.3%和37.5%)。这一结果提示,对于复杂ISR患者,联合技术组的实际临床效果更佳,这为今后治疗1SR提供了新的思路和解决办法。同时我们的初步经验表明,使用联合技术治疗的ISR患者在12个月时获得显著更高的一期通畅率,特别是此次纳入的病例其ISR病变长度为(11.3±8.2)cm,且57.1%的患者为Tosaka分类III。同时发现在Tosaka I级和II级12个月的一期通畅率与Tosaka III级无显着性差异。由于参加该研究的患者数量有限,这并未达到完全统计学意义。
尽管腔内减容联合DCB治疗股腘动脉ISR近期效果显著[21],但也存在一些局限与不足。主要包括远端动脉栓塞[22]、支架断裂以及动脉穿孔[23]、以及患者经济负担的加重。笔者建议合理使用保护伞,特别是对于合并陈旧性血栓、单支流出道病变和严重钙化病变,建议常规使用保护伞,以避免远端栓塞事件的发生。同时在腔内旋切时应选择合适的角度,并结合术前的影像学资料避开重要的分支血管[24]。
本研究表明,腔内减容联合药涂球囊在治疗股腘动脉ISR在近期通畅率方面具有一定的优势,符合目前倡导的“leave nothing behind”理念,减少了支架的再次置入、为未来的再次治疗提供了机会,可作为处理股腘动脉ISR病变的治疗方案之一。然而,本研究纳入的病例数量相对较少,随访时间仅为术后1年,中远期通畅率仍需进一步随访观察。
[1]卫任,郭伟.下肢动脉硬化闭塞症治疗中载药支架的应用现状[J].中国普通外科杂志,2018,27(6):674-678.doi:10.3978/j.issn.1005-6947.2018.06.002.Wei R,Guo W.Application status of drug-eluting stent in treatment of lower extremity arterial occlusive disease[J].Chinese Journal of General Surgery,2018,27(6):674-678.doi:10.3978/j.issn.1005-6947.2018.06.002.
[2]Shishehbor MH.Endovascular Treatment of Femoropopliteal Lesions:So Many Options,Little Consensus[J].J Am Coll Cardiol,2015,66(21):2339-2342.doi:10.1016/j.jacc.2015.09.062.
[3]Kim W,Choi D.Treatment of Femoropopliteal Artery In-stent Restenosis[J].Korean Circ J,2018,48(3):191-197.doi:10.4070/kcj.2018.0074.
[4]Iida O,Soga Y,Hirano K,et al.Long-term outcomes and risk stratification of patency following nitinol stenting in the femoropopliteal segment:retrospective multicenter analysis[J].J Endovasc Ther,2011,18(6):753-761.doi:10.1583/11-3581.1.
[5]Hajibandeh S,Hajibandeh S,Antoniou SA,et al.Treatment strategies for in-stent restenosis in peripheral arterial disease:a systematic review[J].Interact Cardiovasc Thorac Surg,2019,28(2):253-261.doi:10.1093/icvts/ivy233.
[6]Gandini R,Del Giudice C,Merolla S,et al.Treatment of chronic SFA in-stent occlusion with combined laser atherectomy and drugeluting balloon angioplasty in patients with critical limb ischemia:a single-center,prospective,randomized study[J].J Endovasc Ther,2013,20(6):805-814.doi:10.1583/13-4308MR.1.
[7]Jaff M,Dake M,Pompa J,et al.Standardized evaluation and reporting of stent fractures in clinical trials of noncoronary devices[J].Catheter Cardiovasc Interv,2010,70(3):460-462.doi:10.1002/ccd.21240.
[8]符伟国,岳嘉宁.股腘动脉段病变支架内再狭窄的腔内治疗策略分析[J].中华外科杂志,2016,54(8):586-590.doi:10.3760/cma.j.issn.0529-5815.2016.08.006.Fu WG,Yue JN.Analysis of endovascular treatment strategies on in-stent restenosis of femoropopliteal artery lesions[J].Chinese Journal of Surgery,2016,54(8):586-590.doi:10.3760/cma.j.issn.0529-5815.2016.08.006.
[9]佟铸,谷涌泉,郭连瑞,等.腔内斑块切除在缺乏流出道的股腘动脉狭窄病变中的应用[J].中国普通外科杂志,2017,26(6):717-721.doi:10.3978/j.issn.1005-6947.2017.06.008.Tong Z,Gu YQ,Guo LR,et al.Endovascular atherectomy for femoropopliteal artery stenosis with outfl ow obstruction[J].Chinese Journal of General Surgery,2017,26(6):717-721.doi:10.3978/j.issn.1005-6947.2017.06.008.
[10]Ho KJ,Owens CD.Diagnosis,classification,and treatment of femoropopliteal artery in-stent restenosis[J].J Vasc Surg,2017,65(2):545-557.doi:10.1016/j.jvs.2016.09.031.
[11]Tosaka A,Soga Y,Iida O,et al.Classification and clinical impact of restenosis after femoropopliteal stenting[J].J Am Coll Cardiol,2012,59(1):16-23.doi:10.1016/j.jacc.2011.09.036.
[12]Dick P,Sabeti S,Mlekusch W,et al.Conventional balloon angioplasty versus peripheral cutting balloon angioplasty for treatment of femoropopliteal artery in-stent restenosis:initial experience[J].Radiology,2008,248(1):297-302.doi:10.1148/radiol.2481071159.
[13]Zeller T,Dake M D,Tepe G,et al.Treatment of femoropopliteal instent restenosis with paclitaxel-eluting stents[J].JACC Cardiovasc Interv,2013,6(3):274-281.doi:10.1016/j.jcin.2012.12.118.
[14]卢维龙,王兵,吴斐,等.TurboHawk斑块切除系统联合药物涂层球囊在治疗股腘动脉硬化闭塞性疾病中的应用[J].中国普通外科杂志,2018,27(6):692-698.doi:10.3978/j.issn.1005-6947.2018.06.006.Lu WL,Wang B,Wu F,et al.Application of TurboHawk atherectomy device combined with drug-coated balloon in treatment of femoropopliteal occlusive diseases[J].Chinese Journal of General Surgery,2018,27(6):692-698.doi:10.3978/j.issn.1005-6947.2018.06.006.
[15]Brodmann M,Rief P,Froehlich H,et al.Neointimal hyperplasia after silverhawk atherectomy versus percutaneous transluminal angioplasty(PTA)in femoropopliteal stent reobstructions:a controlled,randomized pilot trial[J].Cardiovasc Intervent Radiol,2013,36(1):69-74.doi:10.1007/s00270-012-0479-9.
[16]Mckinsey JF,Zeller T,Rocha-Singh KJ,et al.Lower extremity revascularization using directional atherectomy:12-month prospective results of the DEFINITIVE LE study[J].JACC Cardiovasc Interv,2014,7(8):923-933.doi:10.1016/j.jcin.2014.05.006.
[17]Garcia-Guimaraes M,Antuña P,Maruri-Sanchez R,et al.Calcified neoatherosclerosis causing in-stent restenosis: prevalence,predictors,and implications[J].Coron Artery Dis,2019,30(1):1-8.doi:10.1097/MCA.0000000000000669.
[18]Rosenfield K,Jaff MR,White CJ,et al.Trial of a Paclitaxel-Coated Balloon for Femoropopliteal Artery Disease[J].N Engl J Med,2015,373(2):145-153.doi:10.1056/NEJMoa1406235.
[19]Liistro F,Angioli P,Porto I,et al.Paclitaxel-eluting balloon vs.standard angioplasty to reduce recurrent restenosis in diabetic patients with in-stent restenosis of the superficial femoral and proximal popliteal arteries:the DEBATE-ISR study[J].J Endovasc Ther,2014,21(1):1-8.doi:10.1583/13-4420R.1.
[20]van den Berg JC,Pedrotti M,Canevascini R,et al.In-stent restenosis:mid-term results of debulking using excimer laser and drug-eluting balloons:sustained benefit?[J].J Invasive Cardiol,2014,26(7):333-7.
[21]Kayssi A,Al-Jundi W,Papia G,et al.Drug-eluting balloon angioplasty versus uncoated balloon angioplasty for the treatment ofin-stent restenosis of the femoropopliteal arteries[J].Cochrane Database Syst Rev,2019,1:CD012510.doi:10.1002/14651858.CD012510.
[22]Roberts D,Niazi K,Miller W,et al.Effective endovascular treatment of calcified femoropopliteal disease with directional atherectomy and distal embolic protection:final results of the DEFINITIVE Ca++ trial[J].Catheter Cardiovasc Interv,2014,84(2):236-244.doi:10.1002/ccd.25384.
[23]Stavroulakis K,Bisdas T,Torsello G,et al.Combined Directional Atherectomy and Drug-Eluting Balloon Angioplasty for Isolated Popliteal Artery Lesions in Patients With Peripheral Artery Disease[J].J Endovasc Ther,2015,22(6):847-852.doi:10.1177/1526602815608194.
[24]Rastan A,Mckinsey JF,Garcia LA,et al.One-Year Outcomes Following Directional Atherectomy of Infrapopliteal Artery Lesions:Subgroup Results of the Prospective,Multicenter DEFINITIVE LE Trial[J].J Endovasc Ther,2015,22(6):839-846.doi:10.1177/1526602815608610.
