2018年,国务院明确提出加强临床、科研数据整合共享和应用,加快建设电子健康档案、电子病历等数据库等意见(《关于促进“互联网+医疗健康”发展的意见》)[1]。随着我国互联网科技的发展,大数据分析在医疗领域的应用不断加深。尤其在肿瘤疾病领域,依托于互联网便捷的追踪和数据记录能力,符合数据质控标准的肿瘤登记处数量显著增加(2005年45个至2015年501个)[2-3]。同一时期,我国肿瘤患者诊疗效果也稳步提升,癌症年龄标化病死率逐年下降[4]。
由于分化型甲状腺癌(DTC)良好的生存周期,术后随访和追踪观察需长期投入方可为其诊疗提供质量较高的循证医学证据。但相比于欧美发达国家,我国甲状腺肿瘤数据库的建设起步较晚,高质量的DTC临床研究仍有所欠缺[5]。这也造成国内甲状腺专业协会诊疗推荐多以“专家共识”形式呈现,“实践指南”则较少;即使在少量的指南中,引用基于中国人群队列的参考证据也普遍不足。通过甲状腺肿瘤数据库的建设提升临床研究质量,提供基于国内人群的诊疗指南参考证据亟待解决。鉴于我国庞大的患者群体,互联网的应用无疑是中国甲状腺肿瘤临床研究领域实现弯道超车的重要途径。近年来,众多科技公司和临床中心已着眼于甲状腺肿瘤临床数据库建设布局,人力物力投入持续加大。然而,数据库的挖掘和应用均需以原始临床数据为基础,此层面的质量管理关乎建设临床数据库的成败。
DTC发病率增长迅速,中国年龄标化发病率远高于世界平均水平(10.1/105 vs.6.7/105;2018年),在不同地区有随经济发展程度逐年升高趋势[3,6]。且其诊断和治疗过程单一,预后优良,生存期极长,随访次数随之增多。与其他专业领域相比,我国建设甲状腺肿瘤临床数据库具备专科化程度高(甲状腺专科基本集中在三甲医院)、数据类目少、病例数多等诸多优势。但也存在缺乏模板化的统一建库类目,缺乏数据分级管理质控标准等许多短板;也可能面临后期国内各中心数据库无法整合的困境。本文从临床视角出发,通过甲状腺肿瘤数据库建设过程中的一些问题和思考,分享在甲状腺肿瘤临床数据库质量控制的几点建议,以期为各专业临床数据库的建设提供帮助。
1 建设甲状腺肿瘤数据库的意义和现状
1973年,美国即开始建设监测、流行病学和最终结局项目(surveillance,epidemiology and end results,SEER);1988年美国外科医生学会与癌症协会联合建设国家癌症数据库(National cancer database,NCDB);通过研究者共享计划,来自美国数据库的临床大数据研究成众多肿瘤临床诊疗领域权威指南的参考证据。2007年,日本建设了由397所医疗机构组成的肿瘤登记系统,为以本国居民为研究对象的临床研究提供证据资料[5]。以分化型甲状腺癌(DTC)为例,在目前最具争议的1~4 cm低危DTC手术范围领域,各主要国家(协会)诊疗指南共引用22项临床研究结果作为支持证据,其中18项来源于美国,3项来源于日本[7]。事实上,全世界甲状腺外科的临床实践和科研导向均受临床数据库影响极深。一项美国Tennessee州癌症登记处(数据应用于SEER、NCDB)的调查研究显示,尽管在研究周期内数据完整性和质量均达到国家质控标准,但仍有40%的原发灶手术部位登记有误[8]。因此引发了学界对源于大数据库临床数据质量的反思。
2012年起,我国已陆续建设涵盖28个疾病领域的50个国家临床医学研究中心。天津市肿瘤医院作为国家肿瘤临床医学研究中心,通过深度学习网络的超声诊断模型训练,在甲状腺癌诊断中表现出与影像专家相似的灵敏度和更高的特异度,并在吉林和威海2家医院外部验证中得到认可[9]。仅6年时间(2012年1月—2018年3月),即在甲状腺癌人工智能诊断领域取得较大进步。进一步证实了我国建设甲状腺肿瘤临床数据库重要意义。
临床数据库的优势,一是在于整合多地区临床资源,扩大科研样本量,从而提高临床资源利用度;二是在于多源的信息采集,从而提高数据的完整性。目前我国甲状腺肿瘤数据库的建设,多为计算机技术转码和人工录入两种途径。计算机专家和临床研究者通过对录入数据“二次质控”,以提高数据可挖掘性和满足科研需要。而原始临床信息的质量控制反而可能被忽视。事实上,真实有效的数据是决定肿瘤临床研究成败的关键,也是目前中国甲状腺肿瘤临床数据库建设的痛点。
此外,临床数据库的安全问题必须引起重视。2016年,英国政府出于安全性的担忧,放弃了有争议的医疗档案数据库,并制定了新的安全标准[10-11]。由于随访和科研需要,医疗数据库常涉及大量患者身份及疾病信息,一旦泄露可能对患者生活造成严重影响。《刑法》规定,医疗工作人员将获得的公民个人信息出售或非法提供给他人,情节严重者可处以3年以下有期徒刑。无论通过电子接口传输或人工转录途径建设临床数据库,均应注意信息安全,采取身份信息加密等措施。
2 甲状腺肿瘤临床数据库分级质量控制
甲状腺肿瘤临床数据库主要由住院期间病历(围手术期)信息和随访数据信息构成,两者相辅相成,基本覆盖甲状腺肿瘤诊疗全过程。经过不断提炼,最终形成各项临床研究中的初始特征——中间干预——最终结局这一逻辑链。尽管目前临床研究越来越提倡和重视“原始数据”、“连续病例”等真实世界研究,但在数据提炼、转录过程中,尤其是主观性病历资料转化为客观数据时,不可避免的出现数据损失。甚至可能因数据丢失过多或数据误差而导致研究结果偏差。如何减少数据丢失和误差,是未来建设数据库的重要研究方向。数据库的建设和应用过程即为从原始信息提取为最终科研论文数据的过程,笔者将各级数据库信息特征总结为从0~3级的逐步采录过程(表1)。下一级数据的质量控制依赖于上一级数据的真实性和可利用性。随着患者病例信息数据的逐级转录,数据可利用性逐步上升至可临床科研应用水平(即论著中的各类数据图表展示),而真实性逐渐下降。此过程是临床数据库建设的客观规律,数据库质量控制即为在提高可利用性的过程尽可能保证数据的真实性。
表1 肿瘤临床数据质量分级管理标准
Table1 Hierarchical quality management of cancer clinical database
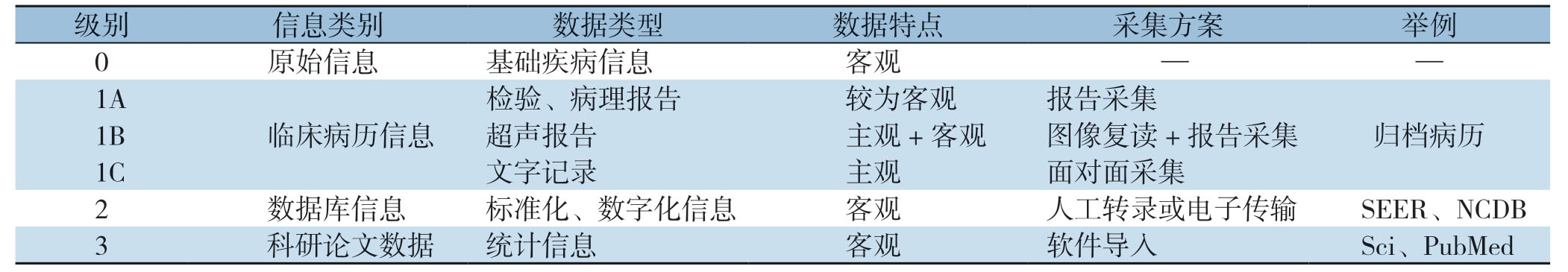
级别 信息类别 数据类型 数据特点 采集方案 举例0原始信息 基础疾病信息 客观 — —1A临床病历信息检验、病理报告 较为客观 报告采集归档病历1B超声报告 主观+客观 图像复读+报告采集1C 文字记录 主观 面对面采集2数据库信息 标准化、数字化信息 客观 人工转录或电子传输 SEER、NCDB 3科研论文数据 统计信息 客观 软件导入 Sci、PubMed
0级数据是患者初始携带的基础疾病信息,通常在门诊、住院初诊时,通过主观表述(主诉)及体征等形式表现,并由接诊医师记录。本级数据具备绝对真实性,但无法直接用于数据库,需经由一线医师转化为具备可利用性的1级数据。
1级数据即为初始病例信息,是对病例原始信息的归纳和总结,可分为两部分——病历信息、手术记录等文字记录,和影像、检验、病理等科室的诊断报告。涉及“主观”数据信息越多,则在此级别数据库建设中数据损失的风险越高,尤其文字记录(1C级数据),一直是临床数据库建设的痛点。患者描述→医生提炼→录入病例框架→人工转录→另一名医生(或科研人员)再次提炼成为可用的数据信息,在此过程中,需要反复多次的文字输出和输入,不同的文字理解和表达能力使数据信息损失的风险大幅增加,数据真实性和可利用性同时下降。而诊断报告尽管均执行各类质控标准,但各单位、各科室质控标准多为各专业间“各自为政”,并未真正意义上结合临床研究需求,采用该专业领域内的整体科研数据质控战略布局。1级病例信息提高标准化、数字化程度,即可极大降低数据信息真实性、可利用性的损失,甚至可在后续各级数据库建设过程中做到“零损伤”的理想状态。此外,随着计算机技术的发展,尤其是OCR(光学字符识别)技术的临床应用,1级病例信息的标准化、数字化,可大幅降低后续各级数据库建设的人力、物力成本。因此提高1级数据质量是提升数据库整体质量的基础和关键所在。
2级数据库可视为临床数据库的“成品”阶段,如SEER、NCDB等肿瘤数据库,均属该范畴。根据各单位信息管理规定不同,多采用人工转录和电子传输等建设方案。此环节的重点在于如何制定合理的数据采集框架。采集数据类目不全,可能在撰写论文中面临补充数据需要,而大数据库的补充数据无疑工作量极大;采集数据类目过多,可能降低数据库的实用性,同样是对劳动成本的浪费。因此,设计2级数据库临床框架前,必须阅读大量临床研究文献,在对临床指南争议和新兴研究方法充分了解基础上,结合单位特色设置2级数据库框架。
3级数据库即为科研成果数据库,包括SCI、PubMed、中国知网等大型的专业文献库。研究者总结经验,通过论文形式分享临床实践及研究成果;同时,又通过各文献的数据展示,吸取经验、了解最新研究动态,从而对后续临床工作进行指导。相较于0、1级数据,3级数据库可利用性极大增加,除一些无法弥补的少量数据缺失外,基本已成为应用便利的科研数据资料。而其真实性问题,更多属科研诚信范畴,本文不作深入探讨。
随着国民文化程度的普遍提高和住院医师规培等项目的施行,在专科化医师和专科化数据库建设的大背景下,0~1级数据转化过程不断优化,已成为具有中国特色临床培养体系的一环。此外,2级数据的管理多依托于科研需求,主要涉及数据采集项目框架,在因人为、技术等因素的真实性和可利用性损失方面并无明显缺陷。因此,笔者结合所在甲状腺中心数据库建设过程中的一些问题,着重探讨1级数据库的建设和质量控制。
3 1级数据库质量的问题与思考
3.1 1A级数据:检验数据
血清甲状腺功能用于指导甲状腺肿瘤术后内分泌抑制治疗,血清甲状腺球蛋白和降钙素等用于监测甲状腺肿瘤术后复发,是甲状腺癌最常用的实验室检查。而国内此类指标的质控尤为混乱。以笔者所在医院为例,甲状腺功能检查即可由检验科、内分泌科、核医学科和产科四个部门执行,包含放免、化学发光和电化学发光三种检测方法。检测仪器、试剂、类目、标准均未统一,且并无校正标准。而基层医院又存在检查项目不全和质控标准不严等问题。不同医院间实验室检查标准差异更加显著,从而为相关多中心研究或联合数据库建设增加巨大障碍。
此外,目前甲状腺癌术后复查项目多以甲功X项等“套餐”形式出现,“同名不同项”屡有发生。除常规指标外,各专科实验室检验侧重点有所不同。如内分泌科甲功监测更偏重于反应甲状腺素循环运载状态的甲状腺结合球蛋白,和反应Graves病自身免疫状态的TSHR-Ab等指标;而核医学科和外科则更偏重于将甲状腺球蛋白作为甲状腺全切术后监测滤泡细胞残余、复发的肿瘤标志物使用。由于患者对术后检测的具体项目缺乏认识,在复查中常出现多做、漏做、误做,及因检测方法不一,前后检验结果难以纵向评估等现象。增加个人经济负担,不利于病情监测,也间接加大了随访门诊工作量。尤其是个别患者可能会因为“号难挂”、“病难看”,甚至认为拿了检验结果医生故意刁难,从而造成医患纠纷。因此,笔者建议同一中心术后复查患者应推荐同一实验室同一检验方法同一检测项目,以便于随访和标准化数据库建设。
手术后6~12个月的甲状旁腺功能和血清钙检测是评估永久性甲状旁腺功能减退和及时改善该并发症群体患者生活质量的重要手段。患者复查过程常无法由其手术医生精准评估,一些术后并发症的评估模式、时间点并未执行统一标准。加之国内分化型甲状腺癌手术多加行中央区淋巴结清扫术,下位旁腺血供损伤风险更高。事实上,由于缺少必要的评价,永久性甲状旁腺功能减退的发生率可能被严重低估。在数据库建设中,应将术后评价指标及时纳入。
3.2 1A级数据:病理数据
病理检查是明确诊断,评估复发/死亡风险和指导下一步治疗的金标准,也是个体化内分泌治疗和随访计划制定的参考。按病理诊断疾病分类,常作为数据库建设的第一要务。2015版ATA指南是推荐证据最为全面和详实的指南之一,共包含101条推荐意见和1 078篇参考文献,是通过甲状腺领域临床研究指导临床实践的标杆。尽管一些研究通过长期随访评价外科结局,但事实上这些研究与具体、详实、高质量的病理学检查密不可分。例如,2012年来自哈佛大学医学院的Randolph等[12]证实PTC淋巴结转移的预后意义可根据淋巴结转移的数量、大小和是否结外侵犯分层。2015版ATA指南随之在复发风险分层中较早前版本作出更新,认为淋巴结转移数量≤5枚且直径≤0.2 cm可归于低危组,而转移数量>5枚或直径>3 cm者则归于中高危组,并将后者命名为高风险N1期(复发率>20%)。由此可见,在临床意义不明确时,美国病理科同道即开始精准评估每一枚淋巴结的形态学特征,付出大量繁琐、枯燥的重复劳动。正因如此,方能推动甲状腺外科临床研究进步。反观国内,2015版ATA指南已发布近5年,大量三甲医院的甲状腺中心,仍无法做到转移淋巴结大小、结外侵犯的评估,甚至淋巴结数量评估也不尽如人意,值得反思。
3.3 1B级数据:超声报告
甲状腺超声是甲状腺结节初始评估的首选方法。所有(已知或怀疑)的甲状腺结节患者均应在初诊时执行甲状腺及颈部淋巴结超声检查和恶性风险分层已在各个国家或地区指南中达成共识。甲状腺影像报告和数据系统(the Thyroid Imaging Reporting and Data System,TI-RADS)是甲状腺超声恶性风险分类的常用方法。2009年Horvarh等[13]首次通过10种甲状腺结节的超声征象定义了TI-RADS分类。随后Park等[14]通过12个超声征象和数学模型建立预测系统,但由于缺乏具体的评分标本和数学模型过于复杂,临床应用较为困难。2018年,美国放射学会(American College of Radiology,ACR)发布基于甲状腺结节超声表现的恶性风险分层系统更新[15]。根据结节成分、回声、形状、边缘和钙化类型五项指标的不同评分将恶性风险由低到高分为1(0.3%)~5级(35.0%),并根据结节不同直径建议是否需执行细针穿刺细胞学诊断(FNAB)。推荐采用结构化标准模板报告每个结节(图1)[16]。韩国甲状腺协会(KTA)及欧洲甲状腺协会(ETA)结合临床研究成果,分别发布了自身的TI-RADS标准(风险区间分别为0~51.3%和0~87.0%)[17-18]。
中国版甲状腺超声TI-RADS分类系统正在筹备中,但迄今为止,我国甲状腺超声报告的TIRADS应用仍非常混乱,不同医院不同医生日常采用何种分类系统,临床医生无法判别。以本中心2019年数据为例,外科医生结合超声报告及二次阅图,在3 111个超声评估结节中TI-RADS分级符合率处于较低水平,超声医生倾向于提供更低的分级报告(44.2%低于Kwak等的分级标准;53.6%低于ACR分级标准),且推荐不同直径结节FNAB评估标准不明。此外,大量多结节病变病例难以准确提供高水平(良恶性特征清晰)、高分辨率的纵横切面图像。在1 043例多结节病变(除外胶质结节)中,仅有47.7%的所有结节进行评估,对临床医生解读超声报告带来极大困扰。因此,FNAB的指征被大幅放宽,“过度诊断”的争议随之而来。
在甲状腺结节初始评估中,超声具有无创、无辐射、价格低廉、操作简便等特点,具有现阶段其他任何检测方法无法替代的优势。但随着FNAB技术的成熟和推广,似乎一些外科医生和超声医生正在忽视超声检测的价值,超声报告质量控制也暴露出不足。。中国人口基数大、病例数众多,此外,随着一些低危结节积极监测方案的实施,需多次超声评估的患者群体可能在未来持续扩大。建立基于中国人群的甲状腺肿瘤超声评价标准,提高超声报告质量,不但是建设临床数据库的基础,也是甲状腺疾病领域实现国家“健康中国规划”的迫切需求。
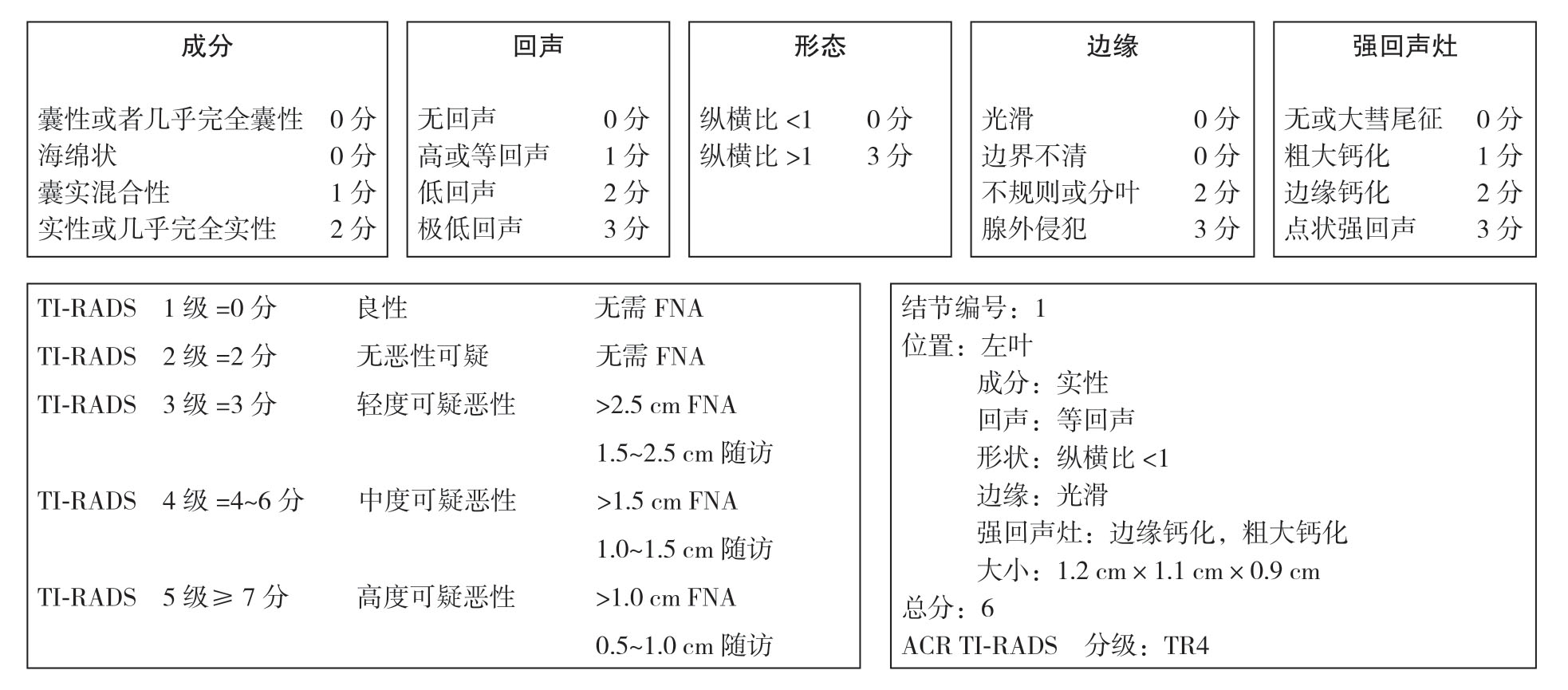
图1 甲状腺结节ACR TI-RADS 外观表现分级及超声报告模板(改编自Franklin 等TI-RADS 使用指南)
Figure1 ACR TI-RADS classification and ultrasound report template for appearance of thyroid nodules (modified from the TI-RADS guidelines by Franklin,et al)
3.4 1C级数据:文字记录
临床数据库中的文字记录主要包括患者病史、体格检查、诊断信息、手术记录和病程记录(并发症记录)等,体现患者的整个入院前和住院期间的疾病管理,是建设原始数据库极为关键的一环。临床医师通常依靠两个步骤完成手术范围决策,一是通过术前体格检查及影像学检查制定初始手术方案,二是根据术中肉眼所见修正。事实上,除我国和日本外,在近几年的DTC诊疗指南更新中,其他主要国家已不再推荐低危分化型甲状腺癌的预防性中央区淋巴结清扫,而更关注于cN1患者治疗性清扫和个性化治疗。体格检查和术中肉眼观察的精确文字记录,与病理诊断结果前后对照,从而汲取经验、弥补缺陷。是临床实践中是提高诊断能力,临床科研中建立预测模型的基础。无论是青年医师成长或数据库建设及后续应用,文字记录均是重要前提。
文字记录涉及到患者的主观表述,临床医生需将复杂、繁琐的病情陈述内容和体格检查结果提炼为可利用数据信息置于病历框架内(如入院记录)。但由于各医生间专科培养、疾病认识、诊疗习惯和关注点的不同,文字记录极难以标准化的方式呈现。此外,与其他语种相比,中文语境对文字含义影响更大,不同人对文字表述、理解的能力差异巨大。这也导致OCR等信息转录技术难以采用,提高数据库建设的门槛,众多单位难以负担数据库建设的高昂人力和经济成本,间接导致科研数据流失。作为普外科的细分学科之一,我国甲状腺中心大多集中在大学教学医院,医教研任务繁重;随着快速康复理念的普及,甲状腺手术病床周转周期极快;医生在病历书写中常常无法投入太多精力,复制粘贴比比皆是。文字记录数据质量难以保证,可能在数据库建设及后续智能化应用场景中造成严重误差。
目前,我国部分医院已开始施行结构化的住院病历、手术记录。通过结构化的1级数据,可使病历信息采集难度大幅降低,甚至信息录入员无需具备医疗专业背景。1级数据库可更简便地转化为标准化、数字化的2级数据库,预期可显著改善整体数据库质量。
标准化数据库的建设对我国甲状腺外科的临床研究发展百利而无一害,通过大数据分析评估既往诊断治疗方案结局,发现问题,从而开展理清临床思路,针对性的制定临床研究方向,可能是目前我国甲状腺外科临床研究最适合的路线。在我国逐步开展“专科医师规范化培训”的契机下,在临床诊疗规范化和计算机技术突飞猛进的背景下,我们正处于改善甲状腺数据库质量,提高临床研究水平的最好时机。多中心协作,多学科合作,共同完善甲状腺专业领域下的临床数据库建设整体布局至关重要。
随着《“健康中国2030规划纲要”》的全面实施,我国医疗+互联网等大健康领域及临床研究中心的发展建设不断渗入,基于大数据的人工智能诊断、疾病预测模型等方向的研究开展如火如荼。此类研究设计均需建立在良好的原始数据库基础上,并投入大量的人力物力。然而原始数据质量不佳,后期几乎无法改善,在大数据库的建设中可能导致“事倍功半”的尴尬局面。事实上,临床数据库的管理缺陷几乎在各个专科领域普遍存在,我们希望以甲状腺肿瘤数据库建设的质量控制为契机,与其他专业领域同道共同探索临床数据库的分级管理模式。笔者也呼吁全国同道,从现在开始重视临床数据管理,共同改善各级数据库质量控制,为我国临床研究提供更精准的数据支持。
[1]中华人民共和国中央人民政府.国务院办公厅关于促进“互联网+医疗健康”发展的意见[EB/OL].国办发[2018]26号.2018–04–28.http://www.gov.cn/zhengce/content/2018–04/28/content_5286645.htm.
Central People's Government of the People's Republic of China.Recommendation of the General Office of the State Council on promoting the development of "internet+medical health" [EB/OL].State Office [2018]No.26.2018–04–28.http://www.gov.cn/zhengce/content/2018–04/28/content_5286645.htm.
[2]Wang J,Yu F,Shang Y,et al.Thyroid cancer:incidence and mortality trends in China,2005–2015[J].Endocrine,2020,68(1):163–173.doi:10.1007/s12020–020–02207–6.
[3]孙可欣,郑荣寿,张思维,等.2015年中国分地区恶性肿瘤发病和死亡分析[J].中国肿瘤,2019,28(1):1–11.doi:10.11735/j.issn.1004–0242.2019.01.A001.
Sun KX,Zheng RS,Zhang SW,et al.Report of Cancer Incidence and Mortality in Different Areas of China,2015[J].China Cancer,2019,28(1):1–11.doi:10.11735/j.issn.1004–0242.2019.01.A001.
[4]Wei F,Wu Y,Tang L,et al.Trend analysis of cancer incidence and mortality in China[J]Sci China Life,2017,60(11):1271–1275.doi:10.1007/s11427–017–9172–6.
[5]程若川,刘文.中国甲状腺癌术后随访和临床研究现状反思[J].中国普通外科杂志,2017,26(11):1375–1382.doi:10.3978/ j.issn.1005–6947.2017.11.002.
Cheng RC,Liu W.Reflections on current problems in postoperative follow-up and clinical study of thyroid carcinoma in China[J].Chinese Journal of General Surgery,2017,26(11):1375–1382.doi:10.3978/ j.issn.1005–6947.2017.11.002.
[6]Observatory.Data source:Globocan 2018.Graph production:Global Cancer[EB/OL].http://gco.iarc.fr.
[7]Liu W,Yan X,Cheng R.Continuing controversy regarding individualized surgical decision-making for patients with 1–4 cm low-risk differentiated thyroid carcinoma:A systematic review[J].Eur J Surg Oncol,2020,46(12):2174–2184.doi:10.1016/j.ejso.2020.08.014.
[8]Kiernan CM,Whiteside MA,Solorzano CC.Cancer Registries:Can We Improve the Quality of Thyroid Cancer Data?[J]Ann Surg Oncol,2017,24(5):1202–1207.doi:10.1245/s10434–016–5612–6.
[9]Li X,Zhang S,Zhang Q,et al.Diagnosis of thyroid cancer using deep convolutional neural network models applied to sonographic images:a retrospective,multicohort,diagnostic study[J].Lancet Oncol,2019,20(2):193–201.doi:10.1016/S1470–2045(18)30762–9.
[10]National Data Guardian for Health and Care.Review of data security,consent and opt-outs[M].www.gov.uk/government/uploads/system/uploads/attachment_data/file/535024/data-securityreview.PDF.
[11]Care Quality Commission.Safe data safe care:report into how data is safely and securely managed in the NHS[EB/OL].www.cqc.org.uk/content/safe-data-safe-care.
[12]Randolph GW,Duh QY,Heller KS,et al.The prognostic significance of nodal metastases from papillary thyroid carcinoma can be stratified based on the size and number of metastatic lymph nodes,as well as the presence of extranodal extension[J].Thyroid,2012,22(11):1144–1152.doi:10.1089/thy.2012.0043.
[13]Horvath E,Majlis S,Rossi R,et al.An Ultrasonogram Reporting System for Thyroid Nodules Stratifying Cancer Risk for Clinical Management[J].J Clin Endocrinol Metab,2009,94(5):1748–1751.doi:10.1210/jc.2008–1724.
[14]Park JY,Lee HJ,Jang HW,et al.A Proposal for a Thyroid Imaging Reporting and Data System for Ultrasound Features of Thyroid Carcinoma[J].Thyroid,2009,19(11):1257–1264.doi:10.1089/thy.2008.0021.
[15]Tessler FN,Middleton WD,Grant EG.Thyroid Imaging Reporting and Data System (TI-RADS):A User's Guide[J].Radiology,2018,287(1):29–36.doi:10.1148/radiol.2017171240.
[16]Middleton WD,Teefey SA,Reading CC,et al.Multiinstitutional analysis of thyroid nodule risk stratification using the American College of Radiology Thyroid Imaging Reporting and Data System[J].AJR Am J Roentgenol,2017,208(6):1331–1341.doi:10.2214/AJR.16.17613.
[17]Yi KH.The revised 2016 Korean Thyroid Association Guidelines for thyroid nodules and cancers:differences from the 2015 American Thyroid Association Guidelines[J].Endocrinol Metab(Seoul),2016,31(3):373–378.doi:10.3803/EnM.2016.31.3.373.
[18]Leenhardt L,Erdogan MF,Hegedus L,et al.2013 European Thyroid Association Guidelines for Cervical Ultrasound Scan and Ultrasound-Guided Techniques in the Postoperative Management of Patients with Thyroid Cancer[J].Eur Thyroid J,2013,2(3):147–159.doi:10.1159/000354537.

